‘GIFT’ 대상품목
의약품(신속심사 대상)
- 심각한 중증 질환 또는 「희귀질환관리법」 제2조제1호에 따른 희귀질환을 치료하기 위한 목적으로 사용되는 의약품으로서, 대체 가능한 의약품이 없거나 대체 가능한 의약품에 비하여 안전성·유효성을 현저히 개선하였거나 개선할 것으로 예상되는 경우
- 생물테러감염병 또는 감염병의 대유행(대유행이 현저히 우려되는 감염병의 발생을 포함한다) 등 공중보건에 심각한 위해를 끼칠 우려가 있는 감염병의 예방 또는 치료를 목적으로 하는 의약품으로서 기존 치료법이 없거나 기존 치료법에 비해 작용 원리ㆍ기전 등이 전혀 새로운 신개념 의약품 또는 기존 치료법보다 유효성 등에서 의미 있는 개선을 보인 경우
- 보건복지부가 지정·공고한 혁신형 제약기업이 개발한 신약
- 신속심사 대상 의약품과 의료기기 조합
*(근거)
「약사법」 제35조의4(우선심사 대상 지정)
「의약품 등의 안전에 관한 규칙」 제40조의2(우선심사 대상 지정)
「공중보건 위기대응 의료제품의 개발 촉진 및 긴급 공급을 위한 특별법」 제7조(우선심사)
첨단바이오의약품(신속처리 대상)
- 대체치료제가 없고 생명을 위협하는 암 등 중대한 질환의 치료를 목적으로 하는 경우
- 「희귀질환관리법」에 따른 희귀질환의 치료를 목적으로 하는 경우
- 「감염병의 예방 및 관리에 관한 법률」에 따른 생물테러감염병 및 그 밖의 감염병의 대유행에 대한 예방 또는 치료를 목적으로 하는 경우
*(근거)
「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」 제36조(신속처리 대상 지정)
「첨단바이오의약품 안전 및 지원에 관한 규칙」 제36조(신속처리 대상 지정)
「첨단바이오의약품의 품목허가·심사 규정」 제21조(신속처리 대상 지정)
‘GIFT’ 지정 신청 절차 및 제출 자료
지정절차
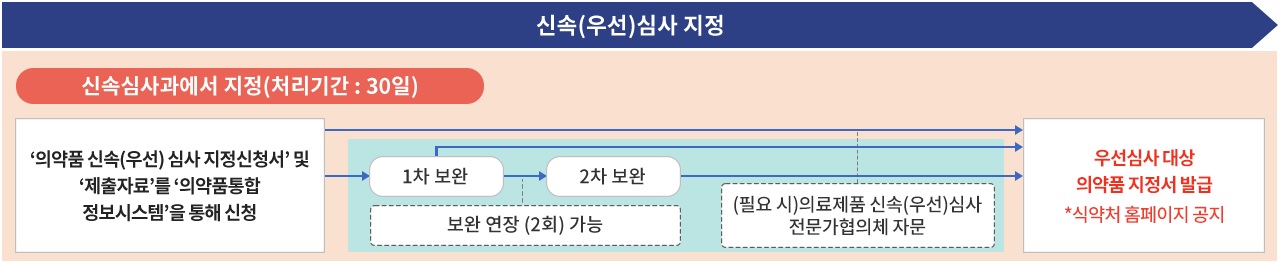 GIFT 품목은 신속심사과에서 지정하며 처리기한은 근무일 기준 30일입니다. 제약사에서 ‘의약품통합정보시스템’을 통해 ‘의약품 신속(우선)심사 지정신청서’ 및 ‘제출자료’를 제출하면, 신속심사과에서 심사를 시작합니다. 심사를 통해 ‘제출자료’가 미흡하여 추가자료가 필요한 경우, 보완요청을 드리며, 자료보완 요청은 2차까지 가능합니다. 자료준비에 시간이 걸리는 경우, 1차 보완요청에 한하여 제출기간을 2회 연장할 수 있습니다. 심사과정에서 필요한 경우, 의료제품 신속심사 전문가협의체의 자문을 받습니다. 이러한 모든 과정이 마무리되어 GIFT 지정이 적합하다고 판단되는 경우, ‘의약품 신속(우선)심사 지정 결과 통지서’와 ‘우선심사 대상 의약품 지정서’를 발급하고 식약처 홈페이지를 통해 지정 품목을 공지합니다.
GIFT 품목은 신속심사과에서 지정하며 처리기한은 근무일 기준 30일입니다. 제약사에서 ‘의약품통합정보시스템’을 통해 ‘의약품 신속(우선)심사 지정신청서’ 및 ‘제출자료’를 제출하면, 신속심사과에서 심사를 시작합니다. 심사를 통해 ‘제출자료’가 미흡하여 추가자료가 필요한 경우, 보완요청을 드리며, 자료보완 요청은 2차까지 가능합니다. 자료준비에 시간이 걸리는 경우, 1차 보완요청에 한하여 제출기간을 2회 연장할 수 있습니다. 심사과정에서 필요한 경우, 의료제품 신속심사 전문가협의체의 자문을 받습니다. 이러한 모든 과정이 마무리되어 GIFT 지정이 적합하다고 판단되는 경우, ‘의약품 신속(우선)심사 지정 결과 통지서’와 ‘우선심사 대상 의약품 지정서’를 발급하고 식약처 홈페이지를 통해 지정 품목을 공지합니다.
- 참고사항
- - 신속(우선)심사 지정대상 의약품은 생물학적제제, 유전자재조합의약품, 한약제제 및 생약제제, 첨단바이오의약품을 포함
- - 관련 법령에 따라 우선심사 대상 의약품 지정서를 발급받은 품목은 신속심사과에서, 이외의 신속심사 대상 의료제품의 경우 의약품심사부, 바이오생약심사부, 의료기기심사부의 각 해당부서에서 수행
- - 첨단바이오의약품의 경우 신속처리 대상 첨단바이오의약품 지정서를 받은 품목은 세포유전자치료제과에서 수행
- GIFT 대상 지정 절차 등에 대한 자세한 내용은 ‘의료제품의 신속심사 지정신청 시 고려사항(민원인 안내서)’를 참고하시기 바랍니다.
- 식약처 대표 누리집(www.mfds.go.kr) → 법령‧자료 → 법령정보 → 공무원지침서/민원인 안내서
제출자료
GIFT 지정 신청 시 다음의 자료를 제출해야 합니다.
- - 신속(우선)심사 대상에 해당함을 입증하는 자료
- - 기원 또는 발견 및 개발 경위에 관한 자료
- - 제조방법에 관한 자료
- - 용법·용량 및 효능·효과에 관한 자료
신속심사(처리) 대상 지정 요약
('20.8.30 ~ '24.2.8.)
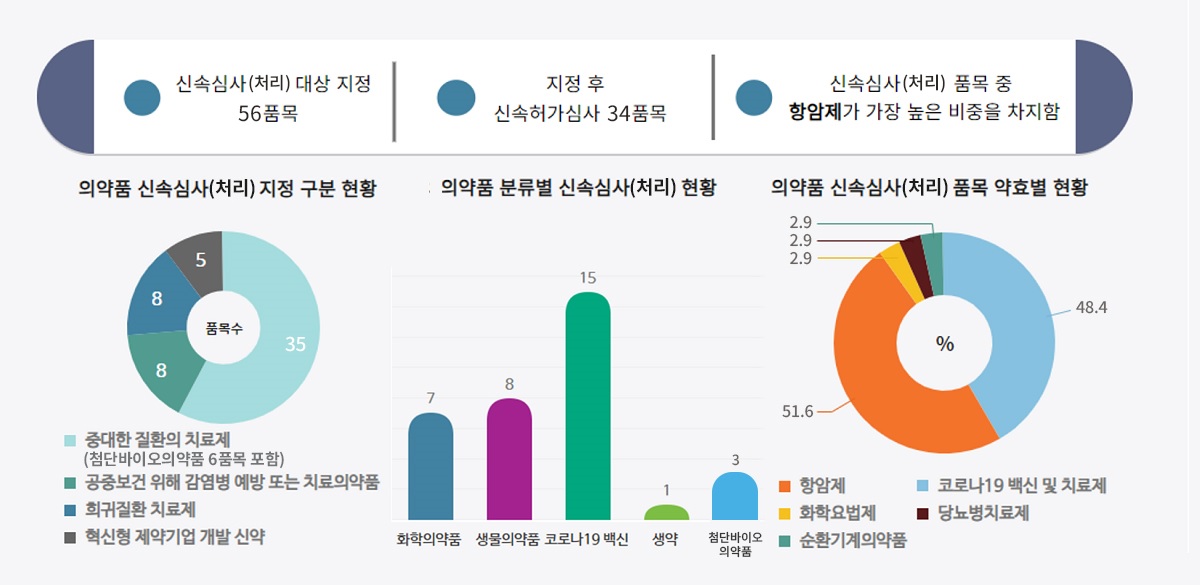
신속심사(처리) 대상 지정 56품목
의약품 신속심사(처리) 지정 구분 현황
- 중대한 질환의 치료제(첨단바이오의약품 6품목 포함):35
- 공중보건 위해 감염병 예방 또는 치료의약품:8
- 희귀질환 치료제:8
- 혁신형 제약기업 개발 신약:5
지정 후 신속허가심사 34품목
의약품 분류별 신속심사(처리) 현황
- 화약의약품:7
- 생물의약품:8
- 코로나19백신:15
- 생약:1
- 첨단바이오의약품:3
신속심사(처리) 품목 중 항암제가 가장 높은 비중을 차지함
의약품 신속심사(처리) 품목 약효별 현황
- 항암제:51.6
- 코로나19치료제백신:48.4
- 화학요법제:2.9
- 당뇨병치료제:2.9
- 순환기계의약품:2.9
 이 누리집은 대한민국 공식 전자정부 누리집입니다.
이 누리집은 대한민국 공식 전자정부 누리집입니다.







